Химические связи в молекулах обычно очень прочны, их энергия находится в пределах 100−150 кДж/моль. Кроме этого существуют так называемые водородные связи, прочность которых составляет 10−40 кДж/моль. Длина этих связей соответственно 270−230 пм.
Водородной связью между атомами Эд и Эв называют взаимодействие, осуществляемое атомом водорода, соединенным с Эд или Эв химической связью.
Изображение водородной связи в общем случае имеет вид ЭА-Н…ЭВ.
Очевидно, что водородная связь трехцентровая, так как в ее образовании принимают участие три атома. Для возникновения такой связи необходимо, чтобы атомы ЭА и Э" обладали большой электроотрицательностью.
Электроотрицательность элемента — способность атомов этого элемента притягивать к себе электроны.
Наиболее электроотрицательные элементы — азот, кислород, фтор и хлор. Водородная связь образуется в результате перекрывания л-АО водорода и двух р-АО атомов ЭА и Эв, образующих водородную связь. /?-Орбитали ориентированы вдоль одной прямой, поэтому водородная связь линейная.
Водородную связь называют: 1) внутримолекулярной, если атомы ЭА и Эв, соединенные этой связью, принадлежат одной и той же молекуле; 2) межмолекулярной, если атомы ЭА и Эв находятся в разных молекулах.
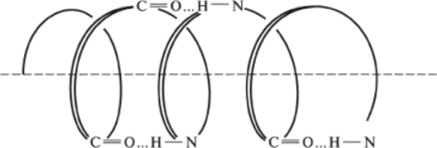
Рис. 1.6. Спиральная структура белковой молекулы.
Внутримолекулярные водородные связи играют важнейшую биологическую роль, так как определяют, например, спиральную структуру полимерных молекул белков. В белках это связи N-H…0 между аминокислотными остатками (рис. 1.6).
Не менее важны межмолекулярные водородные связи. С их помощью соединены цепи нуклеиновых кислот, образующих двойную спираль. Здесь имеются два типа межмолекулярных водородных связей между атомами азота N-H…N и атомами азота и кислорода N-H…O нуклеиновых оснований.
Средняя кинетическая энергия теплового движения молекул имеет значение порядка 3/2RT. При температуре человеческого тела 37 °C (310 К) это составляет около 4 кДж/моль. Прочность водородных связей находится в пределах 10- 40 кДж/моль. Поэтому они достаточно прочны, чтобы выдерживать постоянные удары окружающих молекул и обеспечивать неизменность формы полимерных биологических структур. Вместе с тем при ударах активных молекул водородные связи периодически разрываются, затем вновь восстанавливаются, обеспечивая протекание различных процессов жизнедеятельности.

