Воздействие физико-химических процессов, происходящих в гелях оксигидратов тяжелых металлов (на примере хрома) , на развитие живых организмов (на примере прорастания семян редиса)

Однако, сравнивая образцы № 3 и № 4, можно увидеть, что образец № 4 менее токсичен. Это может быть объяснено тем, что сам по себе коллоидный раствор, содержащий ионы хрома, токсичен вследствие токсичности данного тяжелого металла. Создание потенциала между графитовыми электродами усиливает действие процессов формирования полимерных цепочек, однако в образце № 4 концентрация хрома сравнительно… Читать ещё >
Воздействие физико-химических процессов, происходящих в гелях оксигидратов тяжелых металлов (на примере хрома) , на развитие живых организмов (на примере прорастания семян редиса) (реферат, курсовая, диплом, контрольная)
Е.А. Новосёлова, И. А. Шарфунов, Ю. И. Сухарев Оценка влияния физико-химических процессов в гелях оксигидратов редкоземельных элементов и тяжелых металлов на живые организмы, а также выявление механизма влияния позволяют применять свойства данных систем в сельском хозяйстве для активизации роста и повышения всхожести семян перед посадкой, для уничтожения вредителей (например грибковых), обеззараживания сточных вод птицеводческих хозяйств (влияние на микроорганизмы и глист). Исследования такого рода позволяют лучше понять процессы, происходящие в коллоидных и других гетерогенных системах, а кроме того, получить новые данные о структуре и свойствах воды.
Гель — коллоидная система, в которой образование макромолекул происходит за счет полимеризации гидратированных частиц. Это «живущая» система, свойства которой периодически изменяются во времени. Физико-химические явления, происходящие в гелях оксигидратов тяжелых металлов, весьма сложны. Это химические реакции, структурирование диполей макромолекул, образующих двойной электрический слой (ДЭС), диффузия, определяющая пространственную конфигурацию макромолекул. Свойства и поведение системы определяются концентрацией редкоземельного элемента или тяжелого металла и рН среды, которые влияют на развивающиеся в геле процессы полимеризации, структурирования и последующего разрушения структуры геля, скольжения дисперсной фазы и дисперсионной среды относительно друг друга при трансформации макромолекул [2−3].
Структуры, подобные структурам гелей оксигидратов РЗЭ и ТМ, возникают в воде, которая может быть рассмотрена с точки зрения кластерных моделей. В первом случае вода представлена в виде кластеров из молекул, связанных водородными связями и плавающих в море молекул, в таких связях не участвующих. Модели второй группы рассматривают воду как непрерывную сетку (обычно в этом контексте называемую каркасом) водородных связей, которые содержат пустоты; в них находятся молекулы, не образующие связей с молекулами каркаса.
Для дисперсных гелевых оксигидратных систем характерно структурирование в результате действия между макромолекулами разнонаправленных сил электростатического отталкивания и межмолекулярных сил притяжения Ван-дер-Ваальса. Присоединение и элиминирование мономерного фрагмента, гидратация и дегидратация, протонирование и депротонирование, присоединение и отщепление аниона гидроксила — все это сопровождает рост полимерных цепей оксигидратных форм тяжелых металлов. Данные процессы можно зафиксировать в виде электрических импульсов; «выплески» носят пульсационный характер.
В коллоидной оксигидратной системе макро-молекулярные элементы окружены самопроизвольно сформированным поляризованным диффузным двойным электрическим слоем (ДЭС). Поэтому изменение пространственной ориентации ДЭС (или структуры ДЭС), содержащей ионные заряженные частицы и молекулы воды, должно напрямую оказывать влияние на процессы структурной организации системы в целом.
В ходе эволюции гели оксигидрата хрома претерпевают ряд структурных превращений, вызывающих смену интенсивности действующих в оксигидрате ионно-кластерных потоков. Такие нанокластерные потоки разряжаются на графитовых электродах.
.

Рис. 1. Схематическая запись мицеллы на примере гидрозоля кремния.
Прибор для измерения импульсного поляризационного электрического тока состоял из прямоугольной ячейки, на концах которой закреплялись графитовые электроды (рис. 2). Контакты электродов подключали к электронному регистрирующему блоку. Образцы помещали в эту ячейку. Расстояние между электродами составило 70 мм. Ячейки, содержащие образцы, замыкались практически накоротко, тогда величина выходного сопротивления была незначительной. Возникновение тока в системе фиксировалось снятием показаний с анализируемой среды в течение пяти часов при помощи аналоговоцифрового преобразователя Е-270 с частотой опроса исследуемой системы пять раз в секунду.
Цель: получить данные о влиянии процессов, происходящих в гелях оксигидратов тяжелых металлов (на примере хрома) разных концентраций, на развитие живых организмов (на примере прорастания семян редиса), тока самоорганизации оксигидратных гелей.

Рис. 2. Ячейка для снятия спайковых выплесков.
Задача: провести биотестирование с использованием в качестве тест-объекта семян редиса, характеризующихся высокой отзывчивостью на ингибирующие свойства среды, и определить по результатам опыта, оказывают ли процессы, происходящие в системе, влияние на живые организмы.
Материалы:
- 1. Чашки Петри.
- 2. Марля, фильтровальная бумага.
- 3. Бидистиллированная вода.
- 4. Гель оксигидрата хрома с концентрацией
- 0, 0017 моль/л, значение рН 6,5.
- 5. Гель оксигидрата хрома с концентрацией
- 0, 034 моль/л, значение рН 6,5.
- 6. Семена редиса, сорт «Редис Сакса» .
- 7. Электрохимические ячейки.
- 8. Термостат.
- 9. Регистрирующая аппаратура.
Ход эксперимента. Ингибирующая способность среды определялась нами методом биотестирования, модифицированным и апробированным на кафедре агрохимии МГУ Е. Х. Ремпе и Л. П. Ворониной [1]. Данный метод основан на высокой отзывчивости семян редиса на токсичные вещества и ингибирующее воздействие среды. В качестве тест-объекта были взяты семена редиса сорта «Редис Сакса». Расчет велся путем учета уменьшения длины корней проростков семян в анализируемых образцах по сравнению с контролем. гель оксигидрат редкоземельный организм Для работы взяты восемь стандартных упаковок семян одного сорта из одной партии, семена из всех упаковок перемешаны.
Первоначально был проведен опыт на всхожесть: на двое суток в чашку Петри с лежащей в ней влажной марлей заложили 100 семян. После чего подсчитали ростки. Всхожесть определялась в трех параллелях, средний результат составил 96%. Таким образом, партия семян прошла тест на всхожесть.
Были пронумерованы и подготовлены к работе электрохимические ячейки:
- 1) контрольная проба — бидистиллированная вода в ячейке без графитовых электродов (стеклянный стаканчик);
- 2) бидистиллированая вода с погруженными в нее графитовыми электродами и созданным между ними потенциалом;
- 3) контрольная проба с гелем оксигидрата хрома с концентрацией 0,0017 моль/л без графитовых электродов;
- 4) гель оксигидрата хрома с концентрацией 0,0017 моль/л с погруженными в него графитовыми электродами и созданным между ними потенциалом;
- 5) контрольная проба с гелем оксигидрата хрома с концентрацией 0,034 моль/л без графитовых электродов;
- 6) гель оксигидрата хрома с концентрацией 0,034 моль/л с погруженными в него графитовыми электродами и созданным между ними потенциалом.
В пронумерованные электрохимические ячейки поместили по 15 мл анализируемого или контрольного образца. В ячейки были заложены семена, отсчитанные в количестве 215 штук на каждую ячейку. Ячейки оставили на 24 часа в термостате, для того чтобы семена набухли и началась первая фаза прорастания, которая и определяет воздействие среды на тест-объект. После чего в чистые чашки Петри было уложено по три фильтра, промоченных дистиллированной водой; из стаканчиков семена переносились в чашки по 50 штук, поврежденные семена отбрасывались (четырехкратная повторность). Чашки поместили в термостат еще на двое суток. На третьи сутки мы измерили длину ростков и сравнили величину ростков анализируемого образца с величиной ростков контроля.
Результаты и обсуждение. Эксперимент был выстроен таким образом, чтобы рассмотреть различные варианты поведения систем гелей оксигидрата хрома.
Получены следующие результаты (рис. 3).

Самая большая средняя длина проростков наблюдалась в контрольном образце № 1, в котором семена в первые сутки прорастания находились в бидистиллированной воде без какого-либо влияния на среду извне. Ячейки № 3 и № 5, в которых находился гель оксигидрата хрома в концентрациях 0,0017 и 0,034 моль/л соответственно, оказали ингибирующее воздействие на прорастание семян, что обуславливается токсичными свойствами хрома. Как и ожидалось, при повышении концентрации хрома в анализируемом образце № 5 отмечено не только уменьшение средней длины проростка, но и снижение всхожести семян, которая в ячейке № 5 составила 87%. Если оценивать токсичность данных образцов по эффекту торможения роста корней (по оценочной шкале для данного метода биотестирования), образец № 3 может быть признан умеренно токсичным, а образец № 5 — чрезвычайно токсичным.
При анализе данных по образцам № 1 и № 2 получаем следующее. Погружение в электрохимическую ячейку графитовых электродов и создание потенциала между ними приводит к тому, что процессы, происходящие в бидистиллированной воде, начинают оказывать токсическое действие. Образец № 2 можно охарактеризовать как умеренно токсичный. Особенностью является то, что ингибирующее воздействие среды образца отражается на скорости роста корня, но не на способности к прорастанию, так как всхожесть семян осталась на прежнем уровне — 94−99%. В то же время у семян из образца № 2 снизилась вариативность длины проростка.
Токсичность образца № 4 ниже, чем образца № 3, и образец может быть охарактеризован как малотоксичный. Таким образом, погружение в систему электродов привело к тому, что интенсивность ингибирующего воздействия среды снизилась.
Образец № 6 может быть охарактеризован как чрезвычайно токсичный: помимо торможения роста корня наблюдается снижение всхожести до 60−65%.
Результаты для ячеек № 2, № 4 и № 6 могут быть объяснены при анализе графика зависимости величины токовых выплесков от времени, в течение которого семена подвергались воздействию. На графиках показана зависимость силы тока от продолжительности опыта (I, нА от t, мин). Для образцов № 2 (рис. 4) и № 4 (рис. 5) характерна амплитуда тока в пределах 0,5−1 нА, без скачков. Для образца № 6 (рис. 6) амплитуда составляет порядка 1,5 нА при наблюдающемся скачкообразном росте и падении графика. Ингибирующее или стимулирующее воздействие гелевых систем может быть объяснено воздействием потоков кластеров, которые образуются при изменениях ДЭС в зоне роста семян редиса. Само по себе данное воздействие вызывает негативный эффект, что можно увидеть, сравнивая поведение образцов № 1 и № 2. Негативное воздействие обуславливается увеличением электрической активности в образце № 2 по сравнению с образцом № 1.
Однако, сравнивая образцы № 3 и № 4, можно увидеть, что образец № 4 менее токсичен. Это может быть объяснено тем, что сам по себе коллоидный раствор, содержащий ионы хрома, токсичен вследствие токсичности данного тяжелого металла. Создание потенциала между графитовыми электродами усиливает действие процессов формирования полимерных цепочек, однако в образце № 4 концентрация хрома сравнительно мала, и потому в структуре ДЭС преобладают группы, образованные кластерами воды, которые при «выплеске» и воздействуют непосредственно на зоны роста семян, влияние других процессов при этом снижается и появляется эффект уменьшения токсичности. Кроме того, небольшая концентрация токсичного вещества оказывает стимулирующее действие на защитную (иммунную) систему организма (эффект гомеопатических препаратов).
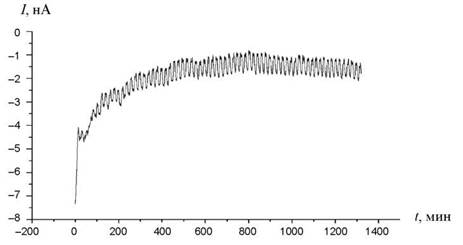
Рис. 4. Зависимость токовых выплесков в образце № 2 от времени.

Рис. 5.
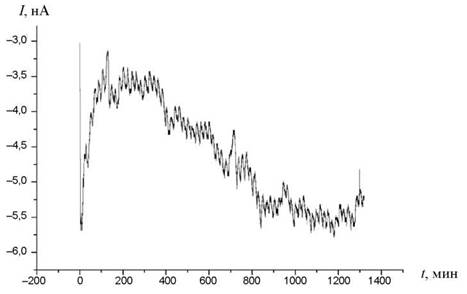
Рис. 6. Зависимость токовых выплесков в образце № 5 от времени.
В образце № 6 концентрация хрома уже существенно выше, в ДЭС появляется больше кластеров, представленных гидратированными частицами хрома, которые начинают участвовать в «выплесках». Теперь на зоны роста семян влияют в основном гидратированные частицы токсичного хрома и мы наблюдаем эффект усиления токсичности. Причем суммируется негативное воздействие матрицы геля и процессов перестройки ДЭС.
Выводы. Процессы полимеризации, структурирования и последующего разрушения структуры геля, скольжение дисперсной фазы и дисперсионной среды относительно друг друга, взаимодействие изменяющихся ДЭС макромолекул во времени оказывают непосредственное влияние на процесс прорастания семян и на их всхожесть.
Отзывчивость семян на ингибирующее или стимулирующее воздействие спонтанных выплесков нанокластеров может быть объяснена стимуляцией или подавлением развития клеток зоны роста корня (проростка) электрическим током. Помимо непосредственного воздействия электричества происходит увеличение или уменьшение токсического эффекта от воздействия ионов хрома оксигидратной матрицы геля, что мы связываем с составом слоев Гуи и Штерна при различной концентрации ионов хрома в гелях оксигидратов хрома.
Условия активизации и подавления роста семян и влияние на их всхожесть интенсивности и частоты токовых выплесков в системе требуют дальнейшего изучения относительно возможности применения данных свойств в сельском хозяйстве для активизации роста и увеличения всхожести семян перед посадкой, а также для уничтожения вредителей.