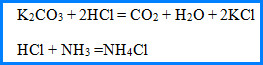Красивые химические опыты
“Огненная метель”
Речь не о природном явлении и не об искрах костра. “Огненная метель” – это название красивого химического опыта. Для его проведения вам понадобятся:
химического опыта. Для его проведения вам понадобятся:
- сосуд объемом более трех литров;
- ложка для сжигания;
- спиртовка или газовая горелка;
- конц. раствор аммиака (или смесь из соли аммония и твердой щелочи);
Сосуд заполните аммиаком одним из способов:
- налейте в него 20 мл концентрированного аммиачного раствора, накройте сверху стеклом и подождите минут 10;
- насыпьте на дно стеклянной емкости смесь из хлорида или нитрата аммония и твердой щелочи (например, NаOH), смочите ее водой и оставьте на некоторое время.
Оксид хрома (III) в ложке для сжигания внесите в пламя спиртовки (горелки). Как только частицы его нагреются докрасна, высыпайте порошок оксида в сосуд с аммиаком. Там крупинки оксида будут раскаляться ещё сильнее и огненными искрами падать на дно.
В основе этого явления лежит процесс окисления аммиака кислородом воздуха под действием катализатора – оксида хрома (III):
Горящие “снежинки” – это частицы катализатора, которые раскаляются ещё больше под действием тепла, полученного при протекании реакции.
Как только горение прекратится, сосуд заполнится бурым газом, а ещё чуть позже – белым дымом. Происхождение их таково:
Белое облако в колбе
С аммиаком можно проводить и другие красивые химические опыты. Например, в любом фильме, будь то сказка, комедия или научная фантастика, в химлаборатории непременно есть колбы, в которых клубится белый дым. Получают его при помощи все того же аммиака.
Для проведения опыта запаситесь колбой и реагентами:
- 10%-ным раствором аммиака;
- концентрированной соляной кислотой;
- твердым карбонатом калия.
 Соль (K2CO3) насыпьте в колбу и залейте аммиачным раствором так, чтобы слой жидкости поверх кристалликов не превышал 2 мм. Сверху аккуратно вливайте кислоту. Вот тогда-то вы и увидите белую струйку “дыма”. Она будет подниматься со дна колбы и под собственной тяжестью оседать по стенкам сосуда вниз.
Соль (K2CO3) насыпьте в колбу и залейте аммиачным раствором так, чтобы слой жидкости поверх кристалликов не превышал 2 мм. Сверху аккуратно вливайте кислоту. Вот тогда-то вы и увидите белую струйку “дыма”. Она будет подниматься со дна колбы и под собственной тяжестью оседать по стенкам сосуда вниз.
Объясняется это неприродное явление просто:
NH3 реагирует с соляной кислотой, образуя белый дым – взвешенные в воздухе частицы хлорида аммония.
Карбонат калия взаимодействует с той же кислотой с образованием другой соли (KCI) и новой кислоты. Однако угольная кислота (H2CO3) неустойчива и тут же разлагается на углекислый газ и воду.
Хлорид аммония образует в воздухе взвесь, а бурно выделяющийся углекислый газ увлекает её за собой. Так как СО2 тяжелее воздуха, то газовая смесь и ползёт вниз.
Как видите, даже самые таинственные и красивые химические опыты представляют собой один – два химических процесса, поэтому повторить их под силу каждому, даже начинающему, химику. Главное, не забывайте соблюдать правила безопасности при работе в химлаборатории. В противном случае чудо закончится трагедией.